مقالات آنالیز و کنترل در آبکاری
تعیین محتوای قلیائیت و مقدار کل چربی در صابونها
- مقالات علمی
- بازدید: 126248
تعیین محتوای قلیائیت و مقدار کل چربی در صابونها
چکیده: محصولات پاک کننده نقش ضروری را در زندگی ما ایفا میکنند. آنها با از بین بردن موثر و ایمن آلودگیها، میکروبها، گردو غبار و غیره به ما کمک میکنند تا زندگی سالمتر و بهتری داشته باشیم. صابون مخلوطی از نمک سدیم اسیدهای چرب گوناگون است. قلیائیت کل و مقدار کل چربی دو پارامتر بسیار مهم در تعیین کیفیت یک صابون میباشند.
لغات کلیدی: صابون، محتوای قلیای آزاد، مقدار چربی کل، صابونی شدن، صابون شستشو
1- مقدمه
صابون درواقع نمک سدیم یا پتاسیم انواع اسیدهای چرب است که حاصل فرایند صابونی شدن یا واکنش هیدرولیز روغنها و چربیهاست. اصولا برای خنثی کردن اسیدهای چرب و تبدیل آنها به به نمکهای مربوطه از سدیم کربنات یا سدیم هیدروکساید استفاده میشود. عمده ترین اسیدهای چرب مورد استفاده در صنایع شوینده و صابون سازی عبارتند از: همانند استئاریک، پالمیتیک، میریستیک، لوریک و اولئیک اسیدها. ویژگیهای شیمیایی صابون به چندین عامل وابسته است: قدرت و خلوص قلیا، نوع روغن مورد استفاده، تکمیل واکنش صابونی شدن و عمر صابون. این خواص شیمیایی عبارتند از: میزان رطوبت، مقدار اسید چرب کلچربی+سود گلیسرول+نمک سدیم اسید چرب
صابون یک سورفکتانت آنیونی است که بدلیل اثر پاک کنندگی که دارد مورد استفاده قرار میگیرد. اگرچه واکنش فوق بصورت یک مرحلهای نمایش داده شده است، اما در واقع یک واکنش دو مرحلهای است. ابتدا و در مرحله اول، پیوند استری شکسته میشود و گلیسرول تبدیل به الکل میشود. درمرحله دوم اسید حاصله در حضور سود به نمک اسیدی تبدیل میشود. در گروه کربونیل یکی از اکسیژنها بواسطه بار منفی که دارد، سدیم با بار مثبت را به سمت خود جذب میکند.
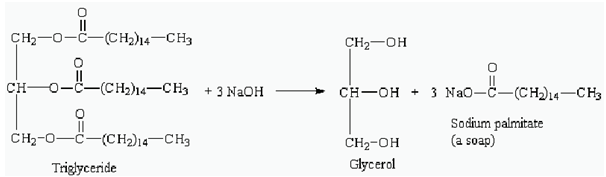
واکنش مربوط به هیدرولیز تریگلیسرید (چربی)
چربیها و روغنهای استفاده شده در صابون عموما منشا حیوانی یا گیاهی دارند. هر چربی یا روغنی مخلوطی از چندین تریگلیسرید است. در مولکول تری گلیسیرید، سه مولکول اسید چرب وجود دارد که به یک مولکول گلیسیرین متصل میباشند. انواع گوناگونی از تری گلیسیریدها وجود دارد. اسیدهای چرب اجزای روغن ها و چربی ها هستند که در ساخت صابون مورد استفاده قرار میگیرند.
محتوای قلیائیت
قلیای مورد استفاده در ساخت صابون را میتوان از خاکتر گیاهان تهیه نمود ولی امروزه میتوان قلیای مورد نیاز بصورت یک محصول تجاری تهیه نمود. قلیاهایی که عموما برای نمکهای محلول مورد استفاده قرار میگیرند قلیاهای فلزاتی چون سدیم و پتاسیم هستند. مهمترین این قلیاها سدسم هیدروکساید و پتاسیم هیدروکساید میباشند. صابونهای پتاسیمی در مقایسه با صابونهای سدیمی به مراتب نرم تر میباشند. در حالیکه صابونهای سدیمی جامد میباشند، صابونهای پتاسیمی بدلیل نرمتر بودن بعنوان صابونهای مایع، خمیر ریش مورد استفاده قرار میگیرند. ترکیب کربوکسیلاتهای سدیم یا پتاسیم موجود در صابون مستقیما به درصد اسید چرب متصل به تری گلیسیرید مربوط میشود. صابونهای حاصل از روغنهای جامد عموما سخت بوده و محتوای نمک سدیمی یا پتاسیمی بالاتری دارند. روغنهای گیاهی بدلیل داشتن اسیدهای چرب غیر اشباع صابونهای نرمی ایجاد میکنند. مطابق استاندارد Bureau از هند (BIS)، یک صابون با کیفیت باید محتوای قلیایی کمتر از 5% داشته باشد در حالیکه طبق ایزو این میزان باید زیر 2% باشد.
مقدار چربی کل
مقدار چربی کل (TFM) یکی از مهمترین ویژگیهای کیفی صابون است و بصورت مقدار چربی کل که عموما بصورت اسید چرب است و میتوان آن را توسط اسید معدنی همانند HCl از نمونه جداسازی کرد، تعریف میشود. اصولا از پارامتر TFM برای بیان سختی و میزان کیفیت صابون استفاده میشود. اسید چرب در صابونهای مخصوص شستشوی بدن عموما نباد TFM کمتر از 78% داشته باشند اما در مورد صابونهای مورد استفاده در صنایع بدلیل صرفه جویی در هزینه تولید از پرکنندهایی استفاده میشود که باعث میشود این عدد حتی کمتر از 50% هم باشد. امروزه در اکثر کشورها صابون با حداقل TFM از نوع صابون درجه یک و با حداقل TFM 65 درجه 2 طبقه بندی میشود و پایین ترین کیفیت صابون مربوط صابون درجه 3 با TFM 50 میشود. هرچه TFM یک صابون بالاتر باشد قدرت کف کنندگی آن بیشتر و پاک کنندگی بهتری برای پوست دارد.
بخش تجربی:
مواد: نمونه صابون، کلروفرم، سدیم هیدروکساید، متیل اورانژ، سدیم کربنات، نیتریک اسید
نکته: سود را با استفاده از محلول استاندارد اگزالیک اسید استاندارد میکنیم و سپس با استفاده از این سود استاندارد شده نیتریک اسید را نیز استاندارد میکنیم.
تعیین قلیاییت کل در نمونه صابون:
برای تعیین قلیائیت کل حدود 5 گرم از صابون (m) را در 100 میلی لیتر آب داغ حل کرده و چند قطره متیل اورانژ به آن اضافه میکنیم. سپس با کمک بورت قطره قطره اسید سولفوریک یا اسید هیدروکلریک 1 نرمال اضافه میکنیم تا تغییر رنگ محلول از نارنجی به قرمز و از لحظه تغییر رنگ محلول حدود 5 سی سی اسید مازاد نیز به محلول اضافه میکنیم و حجم اسید را یادداشت می نماییم (V0). این محلول را حرارت میدهیم به شدت هم میزنیم تا لایه روغنی روی سطح آب تشکیل شود. مخلوط را به یک قیف دکانتور منتقل کرده و سرد میکنیم. با اضافه کردن 50 سی سی پترولیوم اتر فاز روغنی و آبی را کامل از هم جدا میکنیم. با باز کردن شیر دکانتور فاز آبی را خارج میکنیم و مجددا فاز آبی را با پترولیوم اتر شستشو میدهیم. و این فرایند را سه بار تکرار میکنیم. یک روش دیگر هم این است که مخلوط را بعد از تشکیل شدن فاز روغنی بر روی سطح اب داغ کاملا سرد کرده به نحوی که روغن کاملا منجمد شود. به این ترتیب با باز کردن شیر دکانتور فاز ابی خارج میشود و برای اطمینان از باقی نماندن هیچگونه روغنی در فاز آبی آن را با 50 سی سی کلروفرم شستشو میدهیم. سپس فاز آبی را توسط سود 1 نرمال در حضور معرف متیل اورانژ تیتر میکنیم و حجم مصرفی سود را یادداشت میکنیم (V1).
محاسبات:
0.040 * (V0T0-V1T1) * 100/M
در این رابطه:
m= جرم نمونه صابون بر حسب گرم
V0= حجم اسید مصرفی برحسب میلی لیتر
V1= حجم سود مصرفی برحسب میلی لیتر
T0= نرمالیه دقیق اسید
T1= نرمالیته دقیق سود
تعیین محتوای چربی کل
پترولیوم اتر را که در مرحله تعیین قلیائیت جمع آوری کرده بودیم با دقت به یک ظرف با وزن معلوم منتقل میکنیم. در صورت نیاز میتوان محلول را با کاغذ صافی فیلتر هم کرد. سپس تمام پترولیوم اتر را در نهایت احتیاط و با استفاده از یک حمام آب تبخیر میکنیم. باقی مانده را در 20 سی سی اتانول حل کرده، چند قطره معرف فنول فتالئین اضافه میکنیم و با استفاده از محلول هیدروکسید پتاسیوم اتانولی (محلول پتاسیوم هیدروکسید در اتانول) 1 نرمال تا ظهور رنگ صورتی تیتر میکنیم. حجم مصرفی در این مرحله یادداشت شود. سپس محلول اتاولی با کمک حمام آب گرم تبخیر کرده تا کاملا خشک شود برای خشک شدن بهتر کمی استون به آن اضافه کرده وتوسط حمام اب گرم آن را خشک میکنیم. نهایتا باقی مانده را درون آون 103 درجه سانتی گراد گذاشته و تا زمانیکه تغییر وزنی مشاهده نشود خشک شدن ادامه مییابد. سپس برای جلوگیری از جذب رطوبت ظرف را در یک دسیکاتور خنک میکنیم.
[m1 - (V * T * 0038) ] * 100/ m0
در این رابطه:
m0= جرم نمونه صابون بر حسب گرم
m1= جرم صابون پتاسیومی خشک شده بر حسب گرم
V= پتاسیم هیدروکسید اتانولی مصرفی برحسب میلی لیتر
T= نرمالیه دقیق پتاسیم هیدروکسید اتانولی
[1] - total fatty acids
نویسنده این مطلب

محقق واحد پژوهش و گسترش
|
گرد آوری و ترجمه و تدوین : دانش آموخته دکتری شیمی آلی- مهندسی پلیمر دانشگاه شهید مدنی آذربایجان-دانشگاه صنعتی سهند، تبریز- ایران دانش آموخته کارشناسی ارشد شیمی آلی دانشگاه الزهرا (س)-تهران-ایران دانش آموخته کارشناسی شیمی کاربردی دانشگاه تبریز، تبریز- ایران |
Dr. M.J Phd graduated, Organic chemistry- Polymer Engineering Azarbiaijan Shahid Madani University, Tabriz, Iran- Sahand University of Technology, Tabriz, Iran
Alzahra university, Tehran, Iran
Tabriz university, Tabriz, Iran |