مقالات سلامت در آبکاری
HF اسید فلوئوریدریک، کاربردها، خطرات اسیدهای آبکاری- دوزبانه
- مقالات علمی
- بازدید: 129939
اسید های آبکاری، کاربرد ها، خطرات، حفاظت سلامتی
Acids for plating, applications, Safety and Hazards
بخش چهارم:
Chapter Four
اسید هیدروفلوئوریک
| لیست اسید های مورد بررسی | Acids list for review |
|
اسید هیدروفلوئوریک اسید کرمیک اسید اگزالیک |
Sulfuric acid Hydrochloric acid Nitric acid Hydrofluoric acid Acid phosphoric Chromic acid Oxalic acid |
|
properties |
|
| HF | Chemical formula |
| 20.01 g/mol | Molar mass |
| Colorless solution | Appearance |
| 1.15 g/mL (for 48% soln.) | Density |
| −83.6 °C (−118.5 °F; 189.6 K) | Melting point |
| 19.5 °C (67.1 °F; 292.6 K) | Boiling point |
| Miscible. | Solubility in water |
| 3.17 | Acidity (pKa) |
|
مقدمه اسید هیدروفلوئوریک محلولی از هیدروژن فلوراید(HF) در آب است. که آن پیشگام بیشتر ترکیبهای فلوئور دار شامل، داروهایی مثل فلوئوکستین (Prozac) ،مواد گوناگونی مثل PTFE(تفلون)، و خود فلوئور عنصری، است. یک محلول بی رنگ بسیار خورنده است، و توانایی حل بسیاری از مواد بخصوص اکسیدها را دارد. توانایی آن برای حل کردن شیشه از قرن 17 میلادی، حتی قبل از اینکه کارل ویلهلم اسکیل که آن را در مقادیر زیاد در سال 1771 آماده کرد، شناخته شده است.اسید هیدروفلوئوریک معمولا به دلیل واکنش پذیری بالا نسبت به شیشه و واکنش پذیری متوسط نسبت به بسیاری از فلزات، در ظروف پلاستیکی ذخیره می شود (اگر چه کمی به PTFE نفوذ پذیری دارد). |
Introduction Hydrofluoric acid is a solution of hydrogen fluoride (HF) in water. It is a precursor to almost all fluorine compounds, including pharmaceuticals such as fluoxetine (Prozac), diverse materials such as PTFE (Teflon), and elemental fluorine itself. It is a colourless solution that is highly corrosive, capable of dissolving many materials, especially oxides. Its ability to dissolve glass has been known since the 17th century, even before Carl Wilhelm Scheele prepared it in large quantities in 1771. Because of its high reactivity toward glass and moderate reactivity toward many metals, hydrofluoric acid is usually stored in plastic containers (although PTFE is slightly permeable to it). |
|
اسیدیته اسید فلورئوریک به دلیل تعادلی تجزیه شدن آن در آب به عنوان اسید ضعیف دسته بندی میشود.آن در محلول های آبی مشابه طرز اسید های رایج دیگر یونیزه میشود: HF + H2O ⇌ H3O+ + F− HF تنها اسید هیدروهالیدی است که به عنوان اسید قوی در نظر گرفته نمیشود. زمانی که غلظت HF به 100% نزدیک میشود مقدار اسیدیته آن به طرز چشم گیری افزایش میابد زیرا موجب homoassociation میشود: 3 HF ⇌ H2F+ + FHF− آنیون بیفلوئورید (FHF-) با پیوند بسیار قوی هیدروژن-فلورین- هیدروژن پایدار شده است. |
Acidity Hydrofluoric acid is classified as a weak acid because of its lower dissociation constant compared to the strong acids. It ionizes in aqueous solutions in a similar fashion to other common acids: HF + H2O ⇌ H3O+ + F− HF is the only hydrohalic acid that is not considered a strong acid, i.e. it does not fully ionize in dilute aqueous solutions. When the concentration of HF approaches 100%, the acidity increases dramatically because of homoassociation: 3 HF ⇌ H2F+ + FHF− The bifluoride (FHF−) anion is stabilized by the very strong hydrogen–fluorine-hydrogen bond. |
|
روش ساخت اسیدفلوئوریک بوسیله اعمال حرارت از فلورین معدنی (CaF2) با اسید سولفوریک غلیظ تولید میشود. زمانی که این دو در دمای 250 درجه سانتی گراد باهم ترکیب میشوند و واکنش میدهند طبق واکنش زیر هیدروژن فلوراید و کلسیم سولفات تولید میکنند: CaF2 + H2SO4 → 2 HF + CaSO4 اگر چه سنگ معدن فلوئوریت یک پیش ماده مناسب و یک منبع عمده تولید جهانی HF است، HF همچنین به عنوان یک محصول جانبی در تولید اسید فسفریک تولید می شود، که از آپاتیت معدنی استخراج میشود. منابع آپاتیت عموما شامل درصد کمی از فلوئوروآپاتیت میباشد، تجزیه اسید که یک جریان گازهای حاوی دی اکسید گوگرد،آب، HF، مثل ذرات غبار آزاد می کند. بعد از جداسازی جامدات، گازها با اسید سولفوریک و الیوم(به مقاله اسید سولفوریک مراجعه کنید- اسید سولفوریک دودزا) مورد تعامل قرار میگیرند و HF بی آب حاصل میشود. با توجه به ماهیت خورنده HF، تولید آن با انحلال مواد معدنی سیلیکات همراه است و به همین ترتیب مقدار قابل توجهی از اسید فلوروسایلیکیک تولید می شود. |
Methods of Manufacturing Hydrofluoric acid is produced by treatment of the mineral fluorite (CaF2) with concentrated sulfuric acid. When combined at 265 °C, these two substances react to produce hydrogen fluoride and calcium sulfate according to the following chemical equation: CaF2 + H2SO4 → 2 HF + CaSO4 Although bulk fluorite is a suitable precursor and a major source of world HF production, HF is also produced as a by-product of the production of phosphoric acid, which is derived from the mineral apatite. Apatite sources typically contain a few percent of fluoroapatite, acid digestion of which releases a gaseous stream consisting of sulfur dioxide (from the H2SO4), water, and HF, as well as particulates. After separation from the solids, the gases are treated with sulfuric acid and oleum to afford anhydrous HF. Owing to the corrosive nature of HF, its production is accompanied by the dissolution of silicate minerals, and, in this way, significant amounts of fluorosilicic acid are generated. |
|
امنیت و سلامتی اسید فلوئوریدریک علاوه بر این که یک مایع خورنده است، همچنین در هنگام تماس یک سم بسیار قوی است. به علت توانایی اسید فلوئوریدریک در نفوذ بافتی، مسمومیت میتواند به راحتی از طریق تماس با پوست یا چشم، یا زمانی که استنشاق یا بلعیده شود اتفاق افتد. نشانه های قرار گرفتن در معرض اسید هیدروفلوئوریک ممکن است بلافاصله آشکار نشود، و این می تواند قربانیان را به اشتباه اندازد و باعث شود تا درمان پزشکی به تاخیر بیفتد.HF باعث تداخل عملکرد سیستم عصبی میشود، به این معنی که ممکن است سوختگی در ابتدا با درد همراه نباشد.قرار گرفتن در معرض تصادفی می تواند بدون توجه به علائم، باعث تعویق در درمان شود و میزان و شدت آسیب را افزایش دهد.علائم سوختگی با HF شامل التهاب چشم، پوست، بینی و گلو، سوختگی چشم و پوست، رینیت، برونشیت، ادما ریوی (ایجاد مایع در ریه ها) و آسیب استخوان است. |
Health and safety In addition to being a highly corrosive liquid, hydrofluoric acid is also a powerful contact poison. Because of the ability of hydrofluoric acid to penetrate tissue, poisoning can occur readily through exposure of skin or eyes, or when inhaled or swallowed. Symptoms of exposure to hydrofluoric acid may not be immediately evident, and this can provide false reassurance to victims, causing them to delay medical treatment. HF interferes with nerve function, meaning that burns may not initially be painful. Accidental exposures can go unnoticed, delaying treatment and increasing the extent and seriousness of the injury. Symptoms of HF exposure include irritation of the eyes, skin, nose, and throat, eye and skin burns, rhinitis, bronchitis, pulmonary edema (fluid buildup in the lungs), and bone damage. |
|
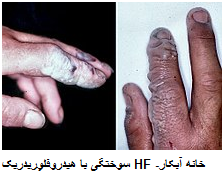
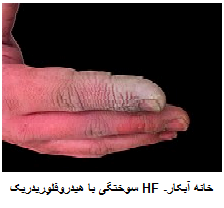
علائم سوختگی با اسید فلورئوریک مولکول هیدروژن فلورئورید بسیار متحرک است که ممکن است به آسانی از پوست حرکت کند. از آنجا که فلوئور تمایل زیادی به ترکیب با کلسیم دارد، استخوان ها مورد حمله قرار می گیرند و این ممکن است منجر به هیپوكالسیمی (کاهش کلسیم موجود در خون) شود.ممکن است درد بلافاصله بعد از سوختگی وجود نداشته باشد، و منجر به زخمی شدن فردی شود که بر این باور است که در خطر نیست. علائم در معرض قرار گرفتن ü غلظت کمتر از 20٪ - erythema (قرمزی پوست) و درد ممکن است تا 24 ساعت بروز نکند، و اغلب سوختگی گزارش نمیشود تا زمانی بافت آسیب شدیدی میبیند. در یک مطالعه مشخص شد علائم٪7 HF 1 تا چند ساعت، 12٪ HF در کمتر از یک ساعت و 5/14٪ HF بلافاصله ایجاد میشود. ü غلظت های 20-50%- erythema و درد ممکن است 1-8 ساعت بعد ایجاد شود، و اغلب تا انجا که بافت آسیب شدید نبیند گزارش نمیشود. ü غلظت های بیشتر از 50%- ایجاد سوختگی بلافاصله میکند،erythema، و آسیب بافتی. |
Symptoms of Hydrofluoric Acid Burns v The Hydrogen Fluoride molecule is so mobile that it may easily pass through the skin.Because Fluorine has an extremely high affinity for Calcium, bones will be attacked,and this may result in hypocalcaemia. There may be no pain immediately after the burn,leading the injured person to believe that they are not in danger. Symptoms of Exposure
|
|
ضد عفونی کردن و کمک های اولیه بلافاصله تمام لباس های آلوده را در آورید، لازم است برای جلوگیری از آلودگی خود اقدامات احتیاطی را رعایت کنی(پوشیدن دستکش) و با مقدار زیادی آب ناحیه آلوده را مورد شستشو قرار دهید. ü 5/2تا 33% کلسیم گلوکنات یا ژل کربناته اعمال شود، پمادر را در دستکش ریخته شود و بعد پوشیده شود یا پماد مستقیما روی ناحیه سوختگیس اعمال شود کلسیم گلوکنات فقط برای اعمال پوستی استفاده میشود. ü از کلسیم کلرید استفاده نشود- کلسیم کلراید بافت ها را تحریک میکند و ممکن است باعث آسیب شود. ü در حالی که قربانی با آب شستشو داده میشود کسی باید با پرسنل پزشکی تماس گیرد و درمان را از آن طریق ترتیب دهد.با 115 تماس گیرد و به وی این موارد را بگوید:
ü پس از اینکه ناحیه سوختگی حداقل یک دقیقه با آب شستشو داده شد، ژل کلسیم کربنات با این راهنمایی باید استفاده شود. یک ژل کلسیم گلوکنات 5/2% باید در داخل کیت مواجهه با HF در آزمایشگاه قرار داده شود. ژل را بعد از پوشیدن دستکش نئوپرن یا نیتریل(22میل) موجود در کیت مواجهه با HF روی ناحیه مورد سوختگی اعمال کنید. از دستکش لاتکس استفاده نکنید. آنها در برابر تاثیر HF مقاومتی ندارد. ساعت اولین اعمال ژل گلوکونات به منطقه آلوده را یادداشت کنید. و این اطلاعات را به تیم اورژانس بدهید. ü قربانی باید توسط یک فرد پاسخ دهنده یا پرسنل آزمایشگاه به بیمارستان انتقال داده شود. ü یک نسخه از MSDS و CHP نیز باید به بیمارستان داده شود. ü پس از رسیدن آمبولانس آنها باید با دکتر اورژانس تماس بگیرند برای تصمیم گیری و دستورالعمل استفاده از قرص کلسیم کربنات موجود در کیت مواجهه با اسید که از آن استفاده کنند. |
Decontamination and First Aid
|
|
کیت در معرض نشت قرار گرفتن قبل از شروع کار با HF، یک کیت مواجهه باید در دسترس و واقع در منطقه آزمایشگاه باشد. کیت قرار گرفتن در معرض باید موارد زیر را شامل باشد: ü ظرف ژل کلسیم گلوکنات
ü 2جفت دستکش نئوپرن یا نیتریل 22 میل ü یک کیسه پلی اتیلنی سنگین برای مواردی که به اسید آلوده شده اند ü یک برچسب آلودگی با HF ü کپی از CHP و MSDS برای انتقال به اتاق اورژانس ü کلسیم کربنات(قرص ضدعفونی کننده) |
the Spill Exposure Kit Before beginning work involving HF an exposure kit must be available and located in the laboratory area. The exposure kit must contain the following items:
|
|
کمک های اولیه برای ü چشم ها را بلافاصله حداقل 5 دقیقه با آب فراوان خنک جریان دارغوطه ور و شستشو داده شود.سپس قربانی باید به یک مرکز پزشکی منتقل شود. اگر محلول استریل کلسیم گلوکنات1% و پرسنل پزشکی دسترس است پس از 5 دقیقه نوبت شستشو، کلسیم کربنات 1% باید شروع شود. ü با شماره 115 تماس بگیرید و به آنها در موردسوختگی با اسید هیدروفلوئوریک اطلاع دهید ومصدوم را با یک شخص مطلع به بیمارستان انتقال دهید. |
First Aid for Eye Exposure
|
|
راه های دیگر قرار گرفتن در معرض سوختگی - عوارض خوردن خوردن آن ممکن است نتایج درد شکمی و استفراغ داشته باشد؛ تاول های ریز دردناک غده گاستریت هموراژیک،و پانکراتیت پس از قرار گرفتن در معرض سوختگی گزارش شده است. |
Other Routes of Exposure - ORAL EXPOSURE
|
|
A hydrofluoric acid burn of the hand |
HF burns, not evident until a day after |
|
شرایط ذخیره سازی هیدروژن فلوراید باید هنگام ذخیره سازی از تماس با فلزات، بابتن، شیشه، و سرامیک اجتناب شود، زیرا میتواند به راحتی به این مواد آسیب برساند. تماس با فلزات ممکن است یک گاز قابل اشتعال ایجاد کند. دور از گرما نگه داری شود. در صورت امکان مایع را به صورت اتومات از بشکه یا دیگر ظروف ذخیره سازی به تانک های فرآیند پمپ کنید.(برای کاهش خطرات تماسی) |
Storage Conditions Hydrogen fluoride must be stored to avoid contact with metals, concrete, glass, and ceramics, because it can severely corrode these materials. Contact with metals may form a flammable gas. Keep away from heat. Where possible automatically pump liquid from drums or other storage containers to process containers. |
|
موارد استفاده: هیدروژن فلوراید در اتچینگ شیشه و صنایع شیمیایی استفاده میشود. هیدروژن فلوراید عمدتا در تولید آلومینیوم و کلروفلوئورو کربنها استفاده میشود. هیدروژن فلوراید همچنین برای جداسازی ایزوتوپ های اورانیوم، بطور مثال کاتالیست در صنعت پترولیوم و اسیدشویی استیل ضد زنگ استفاده میشود. فلوراید گاهی اوقات به آب آشامیدنی عمومی اضافه میشود، و در بعضی تولیدات دندانی استفاده میشود. استفاده های صنعتی:
موارد استفاده مصرف کننده
|
Uses Hydrogen fluoride is used in the glass etching, electronic, and chemical industries. Hydrogen fluoride is predominantly used in the production of aluminum and chlorofluorocarbons (CFCs). Hydrogen fluoride is also used for separating uranium isotopes, as a catalyst in the petroleum industry, and in stainless steel pickling. Fluoride is sometimes added to public drinking water supplies, and is used in a number of dental products. Industry Uses
Consumer Uses
|
|
Reference
|
تهیه شده در واحد پژوهش و گسترش جلاپردازان پرشیا
Prepared by research and development unit of jalapardazan Persia
دی96
نویسنده این مطلب

کارشناس واحد مدیریت کیفیت
کارشناس شیمی دانشگاه شهید صدوقی
همکار در واحد تحقیق و توسعه جلاپردازان از سال 1395